Устройство и история автомобильных аккумуляторов

Аккумулятор электрический (лат. accumulator собиратель, от лат. accumulo собираю, накопляю) — химический источник электрического тока. Главным достоинством аккумуляторов является обратимость химической реакции, т.е. данный источник тока можно не только разряжать, но и заряжать повторно. Благодаря этому свойству аккумуляторы используются в наши дни почти во всех электрических и электронных устройствах — везде, где экономически выгоднее зарядить прежний источник тока, чем покупать новый.
В автомобилях также имеется аккумулятор. Он используется при заводе двигателя, а также в качестве источника электрической энергии на пару с электрогенератором. Однако нужно учесть, что автомобилю требуется ток высокой силы. Одинарный аккумулятор не способен выдать электрический ток достаточной мощности. Для решения этой проблемы используется батарея из соединенных последовательно аккумуляторов. Благодаря такому соединению, как известно из курса физики, происходит сложение силы тока, что дает на выходе достаточную мощность для прокручивания вала двигателя при его заводе.
Отдельные аккумуляторы в батареях сделаны в виде «банок» (ячеек) с помещенными внутри них электродами и залитых электролитом. У каждой «банки» имеется два контакта — положительный и отрицательный. Далее эти контакты последовательно соединены в единую цепь и выведены наружу аккумуляторной батареи в виде общих для АКБ контактов. Каждая такая секция-аккумулятор выдает напряжение в 2 вольта.
Для получения необходимого напряжения в 12 вольт последовательно соединяют шесть таких «банок». Именно на 12 вольт рассчитано электрооборудование почти всех легковых и некоторых легкогрузовых автомобилей. На большинстве тяжелых грузовиков электротехника рассчитана на 24 вольт. Для получения этого напряжения берутся две 12-вольтных аккумуляторных батареи. Для техники, где не требуется высокое напряжение, используются 6-вольтные АКБ (объединены 3 банки по 2 вольта). Данные аккумуляторы устанавливаются на мотоциклах, скутерах, тракторах. Хотя и на этой технике встречаются 12-вольтные АКБ.
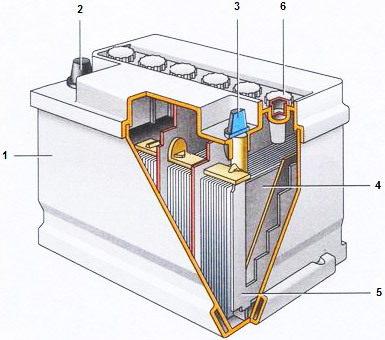
Схема автомобильной аккумуляторной батареи
- Корпус аккумуляторной батареи
- «+» выход АКБ
- «−» выход АКБ
- Анод — положительная пластина
- Катод — отрицательная пластина
- Пробки для обслуживания АКБ
(на необслуживаемых моделях отсутствуют)
Существует множество разновидностей аккумуляторов, различаемых по материалу анода и катода, а также используемому электролиту. В наше время в автомобилях чаще всего используются свинцово-кислотные аккумуляторы, в которых материалом электродов является свинец с разнообразными добавками, а электролитом — водный раствор серной кислоты.
Раньше электроды отливали из чистого свинца, однако он не отличается высокой прочностью и устойчивостью к вибрациям, непременно возникающим при работе двигателя и движении транспортного средства. Поэтому в свинец стали добавлять различные добавки, чтобы увеличить прочность электродов. В качестве такой присадки активно и долгое время использовалась сурьма (в Европе и США — до середины 20 века, в СССР — вплоть до 90-х годов 20 века).
Однако, хоть прочность пластин-электродов и была увеличена, возник побочный эффект — гидролиз воды при зарядке АКБ стал происходить при гораздо более низких значениях напряжения. Из-за гидролиза часть воды улетучивалась в виде газообразных кислорода и водорода. Мало того, что постоянно требовалось следить за уровнем воды в банках, так еще была реальная опасность взрыва, так как кислород и водород, при смешении в определенной пропорции, образуют так называемый «гремучий газ».
Для решения этой проблемы производители применяли различные решения. На некоторых АКБ стали вместо сурьмы использовать добавку из кальция. Это позволило избавиться от повышенного газообразования, но сделало аккумулятор более чувствительным к переразрядам и перезарядам. Наряду с использованием добавок из кальция, также, в качестве альтернативного решения проблемы, стали выпускать малосурьмянистые пластины. Все это позволило увеличить напряжение электролиза с прежних 12 вольт до 16 вольт и выше. А это уже давало возможность свести потери воды практически к нулю, т.е. стал возможен выпуск аккумуляторных батарей, которые не требовали контроля уровня электролита в банках.
Еще одной из проблем являлось постепенное разрушение активной массы и накопление образовавшегося шлама на дне корпуса АКБ и последующее замыкание пластин, вызывающее уменьшение полезной площади, участвующей в накоплении энергии. Первым решением этой проблемы было создание под пластинами специальных канавок, чтобы там могла скапливаться осыпавшаяся активная масса. Разумеется, необходимость резервировать место для шлама приводила либо к увеличению габаритов корпуса АКБ, либо уменьшению полезной площади пластин. И вот было найдено более изящное решение проблемы осыпания электродов: каждую пластину поместили в конверт из пористого материала, свободно пропускающего электролит, но задерживающего частички активной массы электродов. Теперь, даже если происходило частичное осыпание свинцовой смеси с поверхности пластины-электрода, весь этот мусор не падал на дно АКБ, а оставался внутри конверта. Это позволило исключить возможность короткого замыкания. Электроды теперь можно было располагать гораздо ближе друг к другу и крепить прямо ко дну банки. Освободившееся место позволило увеличить полезную площадь пластин.
Но все эти улучшения касались лишь электродов, в то время как электролит — серная кислота — по-прежнему использовался в том же самом виде — в виде водного раствора. Из-за того, что электролит находится в АКБ в жидком виде, с автомобильными аккумуляторами приходится обращаться крайне аккуратно, т.к. серная кислота — агрессивное вещество и способно серьезно повреждать практически всё, что с ней контактирует. Автомобилисты знают, что аккумуляторы крайне нежелательно трясти и наклонять на большой угол, чтобы электролит не проник в каналы в крышке, а потом и наружу АКБ. Также очень опасна была ситуация, когда повреждалась стенка батареи. Электролит вытекал наружу и повреждал все вокруг.
Для решения данной проблемы искали способы отойти от использования электролита в жидком виде. В результате стали использовать серную кислоту в виде геля. В аккумуляторах данного типа кислота загущается до состояния геля путем добавления специального вещества — силикагеля (SiO2). Гелевые аккумуляторы часто можно узнать по обозначению «GEL» на корпусе АКБ.
Еще одной из новинок на рынке является появление аккумуляторов, изготовленных по технологии AGM (Absorbent Glass Mat) — использование абсорбирующего стекломатериала. В АКБ данного типа электролит находится в абсорбированном виде.

AGM аккумуляторные батареи
В гелевых и AGM-аккумуляторах физически отсутствует возможность регулирования уровня и концентрации электролита, т.е. данные АКБ являются полностью необслуживаемыми.
Несмотря на все это великое множество моделей АКБ, в основе их работы лежат одни и те же химические процессы:
При разряде происходит реакция между серной кислотой, оксидом свинца и свинцом. При этом образуются сульфат свинца, выделяется вода и образуется разность потенциалов (электрический ток). В результате разложения серной кислоты и выделения воды снижается концентрация электролита, что может при длительном разряде привести к прекращению работоспособности аккумулятора. Для предотвращения этого не стоит доводить состояние АКБ до полного разряда.
Суммарный химический процесс при разряде аккумулятора:
Pb + PbO2 + 2H2SO4 → 2PbSO4 + 2H2O
При заряде, наоборот, нужно затратить электрический ток для восстановления свинца из сульфата и образования серной кислоты. Это позволяет восстановить концентрацию электролита и подготовить аккумуляторную батарею к повторному использованию (разряду).
Суммарный химический процесс при заряде аккумулятора:
2PbSO4 + 2H2O → Pb + PbO2 + 2H2SO4
Однако не всегда в качестве электролита использовался раствор серной кислоты. Первые аккумуляторы заливались подкисленной водой.
История аккумуляторных батарей отсылает нас в 1859 год, когда французским физиком Гастоном Планте была создана первая аккумуляторная батарея. Химический способ получения электрического тока был известен еще до него: в 1800 году Алессандро Вольта построил свою химическую батарею — знаменитый «Вольтов столб». Но данное устройство получения электричества было однократного действия, не перезаряжаемым.

Аккумуляторная батарея Гастона Планте
Аккумулятор Гастона Планте состоял из пары свинцовых пластин, разделенных тканью и обернутых вокруг деревянного цилиндра. Электролитом была подкисленная вода. Аккумуляторная батарея Планте была дорога в изготовлении и сложна в эксплуатации. Ситуацию изменило изобретение Камилло Фора, работавшего у Гастона Планте и знакомого с его детищем. Фор нашел способ уменьшить стоимость изготовления, а также увеличить энергоемкость аккумулятора. Вместо свинцовой ленты, намотанной вокруг цилиндра, он предложил формировать из свинца решетчатые пластины, покрытые оксидом свинца. Т.е. Камилло Фор получил аккумуляторную батарею практически в том виде, в котором мы ее знаем сейчас.
В наши дни не прекращаются исследования по улучшению аккумуляторных батарей. Изыскиваются способы уменьшения размеров устройства, увеличения емкости и снижения чувствительности к перепадам температуры. Скорее всего, в скором будущем свинцово-кислотные аккумуляторные батареи уступят место в автомобиле более совершенным, построенным по другой технологии. Ну а пока этого не произошло, автомобили будут комплектоваться различными воплощениями старой, свинцово-кислотной, технологии.
Другие статьи
Запчасти в продаже





